Olá pessoal, tudo bem? Hoje no Blog iremos falar sobre os Biofilmes. Você já ouviu falar?
Os biofilmes bacterianos são comunidades formadas por aglomerados de microcolônias de bactérias envoltas por uma matriz extracelular adesiva e fixadas irreversivelmente a uma superfície inerte ou viva [1,3,4]. Mas vamos com calma! Precisamos entender o que leva as bactérias a formarem essas microcolônias…
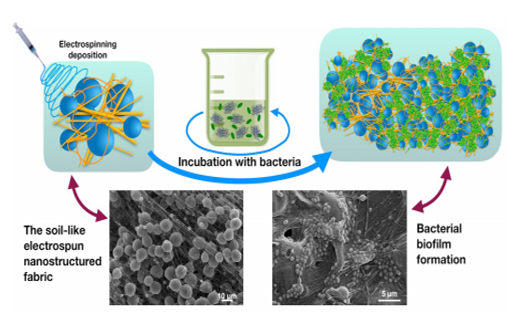
Figura 1: Representação da formação do biofilme [2].
Passeando pela história, podemos perceber como foi a construção de cada passo para que o homem pudesse ter conhecimento acerca dos biofilmes. No século XVII, Anton Von Leeuwenhoek, ao examinar amostras de raspado bucal, notou a presença de células agregadas, após isso, Claude Zobell, em 1943, evidenciou que agregados microbianos marinhos apresentavam certa atração a superfícies, como cascos de navios, vidros, metais e plásticos. Em 1964, foi observado pela primeira vez os estágios iniciais da formação do biofilme, por Ralph Mitchell, mas, somente no ano de 1978, ao pesquisar mais a fundo sobre as comunidades de agregados bacterianos, John William Bill Costerton utilizou o termo biofilme pela primeira vez[1].
Inicialmente acreditava-se que as bactérias existiam de forma individual, onde suas principais atividades compreendiam na busca por nutrientes e proliferação. As bactérias estão presentes em dois tipos de vida, as bactérias planctônicas, que têm o hábito de viver livremente, e as bactérias sésseis, que vivem em comunidade e fixas em determinadas superfícies. É a partir disso que os biofilmes desempenham um papel importante no desenvolvimento das bactérias, pois, quando estas formam as microcolônias, aumentam o seu grau de virulência e patogenicidade[1,4,5].
Sob a forma de biofilmes, as bactérias têm a facilidade de aderência a superfícies, principalmente no ambiente hospitalar. Além disso, são capazes de se proteger contra qualquer agressão externa, dificultando sua eliminação e podem provocar infecções hospitalares e ou acentuar doenças preexistentes. Estima-se que 60% das infecções nosocomiais estão relacionadas ao biofilme e, de acordo com dados de 2007 da Organização Mundial de Saúde (OMS), existem mais de 1.4 milhões de pessoas com infecções nosocomiais[1,6].
Existem diversos tipos de bactérias formadoras de biofilmes, entre as Gram positivas, destacam-se Staphylococcus coagulase negativo e Staphylococcus aureus. As bactérias utilizam um mecanismo de comunicação para se colonizarem, esse mecanismo se chama Quorum sensing.
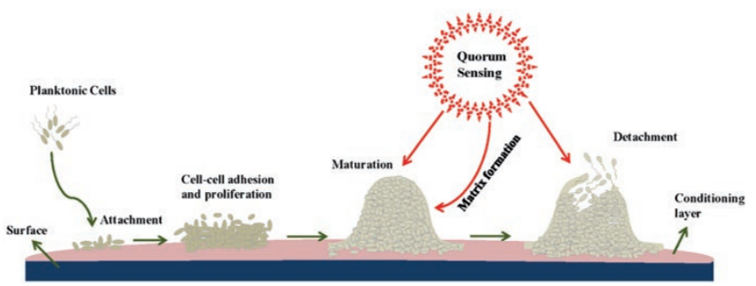
Figura 2: Atuação do Quorum sensing no processo de formação do biofilme [7].
O Quorum Sensing (QS) sendo um mecanismo de sinalização entre as bactérias, produz substâncias semelhantes a hormônios, os autoindutores, que permitem aos microrganismos a identificação e o controle da expressão gênica com base na densidade populacional dentro de um biofilme, promovendo a adaptação ao meio. O mecanismo de QS regula diversos processos fisiológicos, como a bioluminescência, a produção de metabólitos secundários, a indução de esporulação, a motilidade e a produção de exopolissacarídeos. Através desse sistema as bactérias criam uma cadeia de comunicação entre os microrganismos presentes no biofilme para manter a organização populacional, bem como para transmitir sinais para as células quando alguma ameaça é detectada[1].
Para se formar um biofilme tem que passar por vários estágios, vejamos!

Figura 3: Representação esquemática da formação do biofilme bacteriano por estágios . A formação inicia com a fixação reversível de células planctônicas (em marrom oval) seguida de adesão na superfície (cinza) (1). Forma-se uma monocamada de bactérias e fixação irreversível com produção de matriz extracelular (2). Após, uma microcolônia de multicamadas é formada (3). Depois, o biofilme amadurecido forma estruturas ricas em polissacarídeos (4).
O primeiro estágio é conhecido por adesão primária em superfície, também conhecida como adesão bacteriana reversível. E a partir desse estágio as células bacterianas que por algum fator passaram por transformações fenotípicas ou que se encontram em um ambiente hostil migram para determinada superfície, passando a viver de modo séssil, isto é, em comunidade[1,5].
A adesão entre as bactérias e superfícies abióticas acontece por interações físico-químicas não específicas enquanto que a adesão em superfícies bióticas é vista por interações moleculares mediadas por ligações receptor-ligante[1,5].
Já o segundo estágio de formação do biofilme consiste na adesão irreversível ou secundária. Nesse estágio os próprios microrganismos produzem uma substância polimérica extracelular, que além de promover a fixação na superfície, também fixa as bactérias umas às outras. Essa adesão é mediada por interações eletrostáticas ou de Van der Waals, isto é, irreversíveis[1,5].
No terceiro estágio começa a formação de microcolônias como já mecionada, onde o biofilme começa a se estruturar para o seu amadurecimento[1,5].
Agora o biofilme está forte e estável, pois, com a matriz extracelular já determinada, acontece a multiplicação celular para aumentar a população. Nessa fase há um aumento da atividade metabólica, ou seja, há um aumento da capacidade de quebra de enzimas e substratos[1,5].
No quarto estágio, o biofilme adquire uma estrutura firme, tridimensional e heterogênea, semelhante a cogumelos. Essa estrutura possui poros e canais de entrada que funcionam como um sistema de entrada de nutrientes, como oxigênio e metabólitos, além disso serve também como uma barreira contra a penetração de antibióticos. Pode-se perceber que é essa estrutura é um fator de virulência[1,5].
Nessa última fase para formar um biofilme é gerado o QS, como já mencionado. A partir dele são sintetizados os autoindutores (AIs), compostos esses que criam uma cadeia de comunicação entre as bactérias envolvidas no biofilme para manter a organização populacional mais forte, e, para isso, há uma transmissão de sinais para as células quando ocorre alguma ameaça[1,5].
Nesta fase pode acontecer de algumas bactérias que estavam em estado de dormência serem expulsas pelo motivo da alta densidade populacional e falta de nutrientes. Elas podem formar um novo biofilme em outros locais[1,5]. Essas células que foram liberadas, são mais virulentas que as células da comunidade anterior, pois quando se encontram em estado de dormência adquiriram genes de resistência, o que torna essas bactérias mais resistentes ao efeito dos antibióticos[1,5,6].
Em resumo, hoje aprendemos um pouco mais sobre os biofilmes e como eles desempenham um papel importante quanto a infecções. Compreendemos que eles têm um meio de comunicação chamado de quorum sensing, que o tornam mais resistentes. Além disso, mostramos que há dificuldade da ação do antibiótico quando há uma formação de um novo biofilme, pois o QS contribui para a adaptação rápida dessas bactérias. Nesse contexto, ressalta-se a necessidade de mais estudos nessa área para obtenção de estratégias e tecnologias que evitem ou possam controlar a formação de biofilmes.
Referências
- Da Silva, Amanda Sales et al. (2020)Quórum sensing e suas implicações na formação de biofilme bacteriano em hospitais. Journal of Infection Control, v. 9, n. 1, p. 37-42.
- De Cesare, Fabrizio et al.(2020) A 3D soil-like nanostructured fabric for the development of bacterial biofilms for agricultural and environmental uses. Environmental Science: Nano, v. 7, n. 9, p. 2546-2572. https://doi.org/10.1039/D0EN00268B.
- Goncalves, Thaís Gonçalves; TIMM, Cláudio Dias. (2020). Produção de biofilme por Staphylococcus coagulase-negativo: uma revisão. Arq. Inst. Biol. , São Paulo, v. 87, e1382018. Disponível em <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1808-16572020000100600&lng=en&nrm=iso>. acesso em 29 de outubro de 2020. Epub 20 de julho de 2020. https://doi.org/10.1590/1808-1657001382018.
- Mirzaei, R., Mohammadzadeh, R., Sholeh, M., Karampoor, S., Abdi, M., Dogan, E., … & Yousefimashouf, R. (2020). The importance of intracellular bacterial biofilm in infectious diseases. Microbial Pathogenesis, 104393. https://doi.org/10.1016/j.micpath.2020.104393.
- Xu, Y., Dhaouadi, Y., Stoodley, P., & Ren, D. (2020). Sensing the unreachable: challenges and opportunities in biofilm detection. Current opinion in biotechnology, 64, 79-84. https://doi.org/10.1016/j.copbio.2019.10.009.
- Zhao, F., Yang, H., Bi, D., Khaledi, A., & Qiao, M. (2020). A systematic review and meta-analysis of antibiotic resistance patterns, and the correlation between biofilm formation with virulence factors in uropathogenic E. coli isolated from urinary tract infections. Microbial Pathogenesis, 104196. https://doi.org/10.1016/j.micpath.2020.104196.
- Subramani R., Jayaprakashvel M. (2019) Bacterial Quorum Sensing: Biofilm Formation, Survival Behaviour and Antibiotic Resistance. In: Bramhachari P. (eds) Implication of Quorum Sensing and Biofilm Formation in Medicine, Agriculture and Food Industry. Springer, Singapore. https://doi.org/10.1007/978-981-32-9409-7_3