Olá pessoal, tudo bem com vocês?
Vamos dar sequência aos ensaios pré-clínicos e as atividades que podem ser analisadas, nele?
Podemos analisar a: toxicidade de um novo composto e para isso existem inúmeros tipos de ensaios, vamos aprender um pouco mais?
Ensaios de toxicidade
A toxicologia se baseia em dois tipos de relação, uma delas se dá entre a quantidade da substância ingerida, ou seja, a dose e a alteração biológica causada ao organismo… essa relação é chamada relação dose-efeito [1,2].
Por outro lado, a outra relação determina a quantidade de organismos de uma população que apresenta efeitos depois da exposição à uma determinada substância. Relação chamada dose resposta [1,2].
Vocês acham que toda substância pode ser considerada um agente tóxico?
Isso depende muito das condições de exposição, do tempo, da via de absorção, frequência e concentração da dose [3].
Portanto… é fundamental conhecer as condições de uso seguro de substâncias para a saúde da população. Vejamos que por um lado toda substância pode ser tóxica… ou toda substância pode ser usada de forma segura. E para isso existe uma forma de calcular a dose de um agente tóxico… [3].
E essa forma é observando na relação dose-resposta:
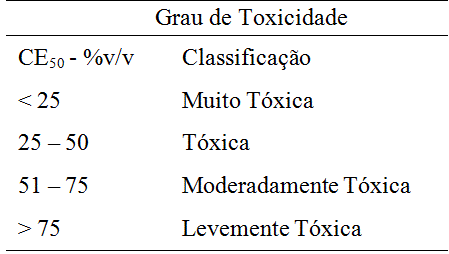
Onde a relação entre a concentração exposta e os efeitos tóxicos são observados, como a DL50, isto é, a dose que pode levar a morte de 50% de uma população em condições experimentais. Observe o grau de toxicidade na Tabela 1 logo abaixo [4].
Classificação da toxicidade
Tabela 1 Faixas de toxicidade [4].
Foi em 1981 que a Organização para Cooperação Econômica e Desenvolvimento (OECD), incorporou o teste da dose letal mediana (DL50) e criou a diretriz 401, que recomendou a redução de animais, empregando apenas 30 para a avaliação da toxicidade oral aguda de um novo agente químico. Na década de 90 a (OECD) criou três métodos para a determinação da DL50: o teste de dose fixa, o método de toxicidade aguda de classe e o método up and down. [6]. Mas o que iremos abordar é o teste de dose fixa.
A partir da DL50 é possível estabelecer a dose limite…
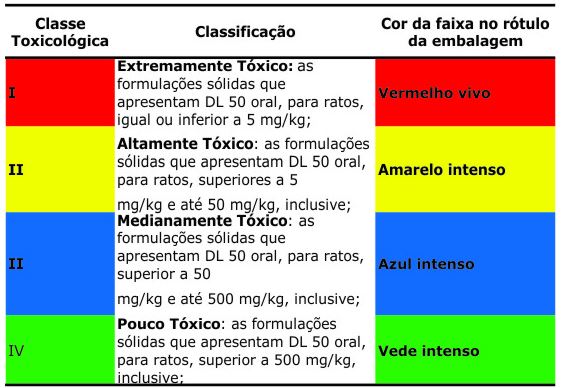
E também a dose mínima necessária para produzir uma resposta detectável em uma população teste. Outra forma de avaliar é a partir do teste de dose fixa onde a substância a ser testada é administrada em um animal em uma dose específica [3].
Tipos de teste toxicológico
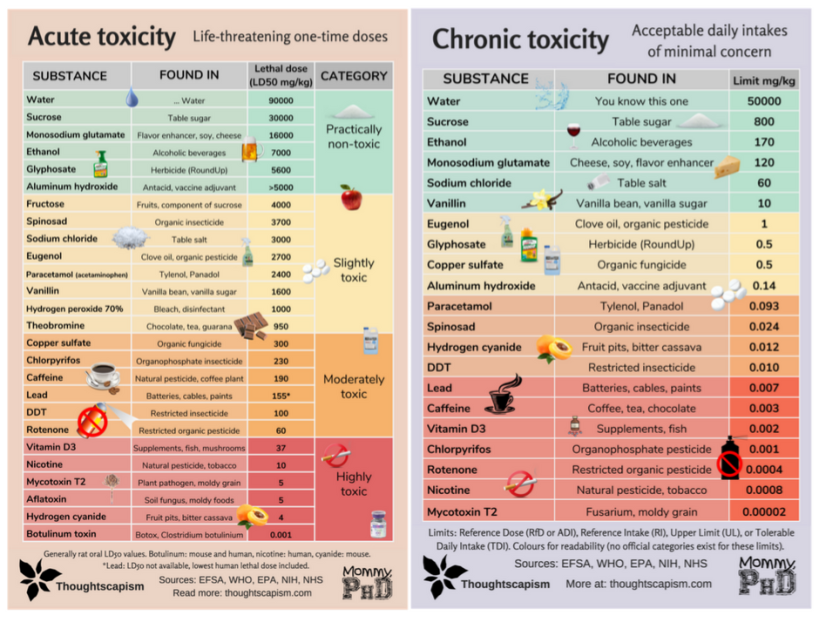
Para se conhecer os efeitos tóxicos de uma substância, além da dose-resposta, é recomendado realizar testes toxicológicos. Temos:
- Toxidade Aguda;
- Toxidade Subcrônica;
- Toxidade Crônica;
- Teratogenia;
- Embiotoxicidade.
E ainda mais, temos também:
- Informações preliminares;
- Toxicocinética;
- Fertilidade;
- Peri e pós-natal;
- Genotoxicidade;
- Carcinogênese e mutagênese;
- Imunotoxicidade.
Toxicidade aguda
A avaliação da toxicidade aguda é empregada para classificar substâncias de acordo com o seu potencial de toxicidade ou letalidade. Como estudos toxicológicos realizados em animais de laboratório e sob condições previamente planejadas, possibilitam definir possíveis efeitos de tais substâncias em seres expostos às mesmas [6].
Ela tem a finalidade de apontar as reações adversas em curto prazo após a administração de um composto. A determinação desse teste pode ser definida a partir dos efeitos adversos que acontecem dentro de um período de 24 horas após a administração de uma única dose ou de doses múltiplas. Um exemplo é a exposição aguda por inalação, refere-se à exposição contínua por menos de 24 horas, mais frequentemente por 4 horas [6].
Toxicidade subcrônica
Tem a finalidade de obter informações de toxicidade após exposições repetidas que ocorrem de 21 a 90 dias. É necessário observar os tecidos afetados no médio prazo, pois pode haver ou não haver o acúmulo da substância no organismo [4].
Toxicidade crônica
É um teste que determina efeitos tóxicos após exposição prolongada, sendo semelhante ao teste subcrônico, a diferença apenas é o período maior, é de 2 anos, utilizando 3 níveis de doses da via de administração usada pela substância química [4].
Teste de teratogenia
É um teste realizado a partir de um protocolo dividido em três fases, nas quais são:
- Avaliação do potencial tóxico da substância sobre a fertilidade e o desempenho reprodutivo;
- Avaliação através de doses diárias da substância química na dieta de fêmeas grávidas;
- Avaliação do desenvolvimento peri e pós natal, com administração da substância química no último terço da gestação até o desmame, onde se avalia o desenvolvimento somático, neuromotor, sensorial e de comportamento dos filhotes [4].
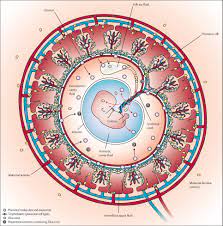
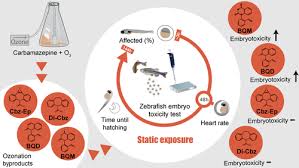
Embriotoxicidade
Para realizar uma avaliação do efeito tóxico de um agente químico durante a gestação, é necessário verificar a toxicocinética, pois ela pode se modificar durante a condição fisiológica que envolve a unidade “materno-placentária-fetal”. Se por acaso aparecer um efeito embriotóxico de uma substância química nessa gestante, há uma grande probabilidade de malformações, déficit funcional, retardo no desenvolvimento geral ou especifico ou até mesmo a letalidade, dependendo do tipo de agente, da dose e frequência de exposição e da idade gestacional no qual se encontra o concepto no momento da exposição [7].
Informações preliminares
São informações que possui a finalidade de saber mais sobre a substância antes da realização dos testes, e por isso deve-se:
- Conhecer a estrutura química;
- Saber se contém ou não impurezas;
- Verificar propriedades físico-químicas, como por exemplo: odor, cor, densidade, viscosidade, solubilidade, volatilidade e etc…
- Observar o quanto essa substância é exposta à população.
Toxicocinética
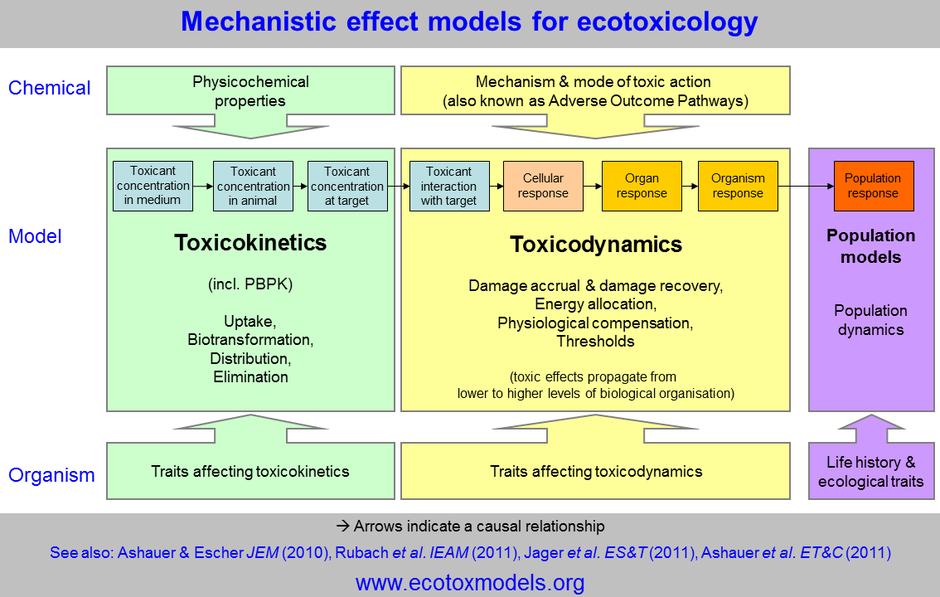
É a avaliação da disposição cinética de uma substância química ou xenobiótico, definida através de ações como: absorção, distribuição, biotransformação e eliminação pelo organismo. Vejamos abaixo as etapas percorridas [1]:
Absorção no organismo é processo que ocorre na passagem do agente tóxico do meio exterior para o meio interior, ou seja, para a corrente sanguínea, através de vias extravasculares inalatória, dérmica e oral [3].
Distribuição acontece quando uma substância no organismo entra em processo dinâmico dependendo da afinidade pela substância. Uma vez no sangue, a substância de distribui em frações para ser transportada pelos glóbulos (fração globular, fase lipídica) e a fração plasmática (fase aquosa), conforme as suas características físico-químicas [3].
Biotransformação é compreendida por várias alterações estruturais ou químicas das substâncias toxicas dentro do organismo, um processo que leva o metabolismo converter essas substâncias lipossolúveis em grandes metabólitos hidrossolúveis para serem eliminados com maior facilidade [3].
Eliminação é o processo final para desaparecer uma substância do corpo. Pode ser por excreção ou por transformação em outras substâncias [3].
Diante dessas etapas, a coleta seriada de amostras de sangue e plasma é considerada um método mais simples e menos invasivo para a obtenção de informações sobre os processos de absorção, distribuição, biotransformação e eliminação de uma substância no organismo [1].
Fertilidade
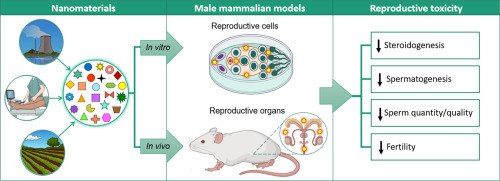
Para a avaliação da fertilidade existe critérios da qualidade do cultivo dos organismos que são utilizados em testes de toxicidade, associado ao teor de lipídeos acumulados no organismo e também a sensibilidade a substância utilizada. Ele depende muito do tipo de estudo a ser realizado [8].
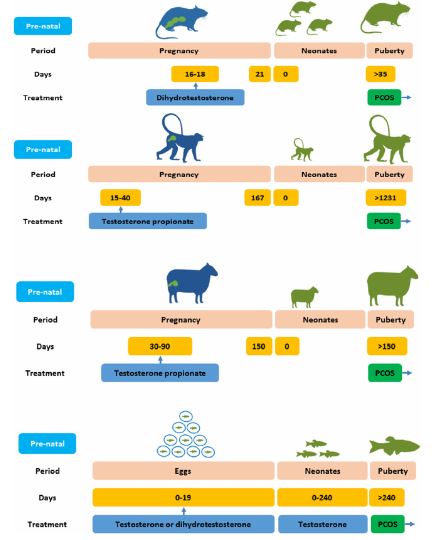
Peri e pós-natal
Durante o período pré e pós-natal, substâncias tóxicas presente no sangue materno através da placenta, período gestacional ou no leite materno durante a lactação, tem uma maior exposição pela baixa capacidade metabólica e excretora e ausência de mecanismos do sistema endócrino [9].
E é nessas fases em que os órgãos sexuais e o sistema nervoso central dos animais ainda estão em desenvolvimento, por isso o tratamento dos machos antes da concepção pode trazer resultados como a infertilidade, morte embrionária ou até mesmo anomalias não especificas, e outras consequências como redução do peso ao nascer, diminuição do tamanho da ninhada e retardo do desenvolvimento pós-natal [9].
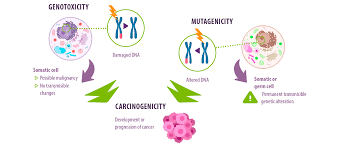
Genotoxicidade
Este teste tem a finalidade de avaliar os indicadores de genotoxicidade, efeitos de exposições ao material genético por meio da avaliação de mutação gênica, dano cromossômico ou lesão no DNA. Alguns ensaios dessa avaliação também compreendem a troca de cromátides irmãs, aberrações cromossômicas (ACs), mutações pontuais e oncogênicas, micronúcleos e o ensaio cometa, sendo este último utilizado para avaliar lesões no DNA5-8 [6, 11,12, 13].
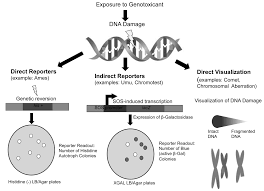
Teste de Mutagenicidade
É um ensaio que avalia os efeitos mutagênicos das substâncias químicas. Realizados através dos microrganismos in vitro, e também em outros organismos [6].
Este teste:
- Avalia o dano provocado na molécula de DNA pela substância química;
- Prever o desenvolvimento do câncer;
- Quantificar o perigo da lesão ao material genético;
- Avalia alterações nos espermatozoides;
- Avalia o desenvolvimento do embrião e feto;
- Prever o desenvolvimento do câncer.
Imunotoxicidade
A avaliação da imunotoxicidade começa pela exposição da substância química por pelo menos 28 dias, seguindo-se a avaliação da resposta humoral. Visto que se o composto produz supressão significativa da resposta humoral, é realizada a avaliação de marcadores celulares por citometria de fluxo. Por outro lado, se o composto não produz supressão de resposta humoral, a avaliação da imunidade inata (ensaio de células NK) deve ser feita [1].
Modelos de animais em Imunotoxicologia
Para essa avaliação é recomendada a realização em modelo animal, preferencialmente em ratos ou camundongos, pois eles possuem [1]:
- Uma quantidade disponível de informações relevantes sobre seu o sistema imune;
- Para seu manuseio o seu custo de manutenção é menor do que de animais maiores;
- Uma vasta variedade de reagentes murinos (citocinas e anticorpos) com fácil disponibilidade.
Incrível ver como esses ensaios são úteis para a saúde da humanidade e auxiliou em inúmeros novos fármacos, assim como a aplicabilidade na população.
Legal, ne?
Gostou? Deixe seu comentário e compartilhe com os colegas.
Até a próxima!
Referências
- KLAASSEN, Curtis D.; WATKINS III, John B. Fundamentos em Toxicologia de Casarett e Doull (Lange). AMGH Editora, 2009.
- CAZARIN, Karen Cristine Ceroni; CORRÊA, Cristiana Leslie; ZAMBRONE, Flávio Ailton Duque. Redução, refinamento e substituição do uso de animais em estudos toxicológicos: uma abordagem atual. Revista Brasileira de Ciências Farmacêuticas, v. 40, n. 3, p. 289-299, 2004.
- Peruzzo, Lucile Cecília. Toxicologia e segurança. Indaial: UNIASSELVI, 2018
- SPRADA, Edilmere. Toxicologia. 2018.
- Campos, Fábio, & Roque Passos Piveli. “Redução da toxicidade aguda de lixiviado de aterro sanitário em co-tratamento com esgoto doméstico pelo processo integrado de lodo ativado com biofilme em leito móvel.” Revista Ambiente & Água 11.2 (2016): 316-326.http://dx.doi.org/10.4136/ambi-agua.1835.
- PAIXÃO, Monique de Sousa. Avaliação da Toxicidade do extrato Hidroalcoólico da entrecasca de Croton argyrophyllus Kunth. 2018. Dissertação de Mestrado. Universidade Federal de Pernambuco.
- PINTO, Flávia Cristina Morone et al. Estudo da embriotoxicidade da beta-ionona em ratos. 2005. Tese de Doutorado.
- BEATRICI, Aline Cristina. Avaliação da fertilidade e sensibilidade de Daphnia similis (Crustacea, Cladocera) submetida a três diferentes dietas. 2000. Tese de Doutorado. Dissertação de Bacharelado, Ufrgs, Porto Alegre, Brazil.
- HOLLENBACH, Clarissa Boemler et al. Desenvolvimento pós-natal e potencial teratogênico da prole de ratos Wistar no estudo da toxicidade reprodutiva de duas preparações fitoterápicas contendo soja Glycine max (L.) Merr. Arquivo Brasileiro de Medicina Veterinária e Zootecnia, v. 62, n. 4, p. 845-852, 2010.
- CANESIN, Renato, et al. “Psicotrópicos: revisão de literatura.” Revista Científica Eletrônica de Medicina Veterinária 6.11 (2008): 41-7.
- Valente, Daniel, et al. “Utilização de biomarcadores de genotoxicidade e expressão gênica na avaliação de trabalhadores de postos de combustíveis expostos a vapores de gasolina.” Revista Brasileira de Saúde Ocupacional 42 (2017).
- Schnaider, Taylor Brandão, & Cláudio de Souza. “Aspectos éticos da experimentação animal.” Revista Brasileira de Anestesiologia 53.2 (2003): 278-285.
- DE QUEIROZ, Anderson Pinto Alves et al. “BIOÉTICA NO USO DE ANIMAIS EM EXPERIMENTAÇÃO.” Ciência Atual–Revista Científica Multidisciplinar do Centro Universitário São José 13.1 (2019).



