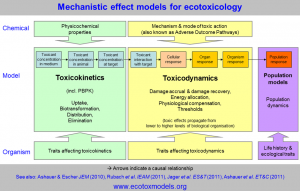
Os antimicrobianos são substâncias que podem ser de origem natural ou sintética. São capazes de inibir o crescimento ou causar a morte de agentes externos como fungos e bactérias. Eles podem atuar de duas formas distintas: a bacteriostática, quando apenas inibe o crescimento bacteriano, mantendo as bactérias em fase estacionária, ou seja, de forma inerte; e a bactericida, quando mata os microrganismos de forma direta, agindo em reações vitais para a célula infectante [1]
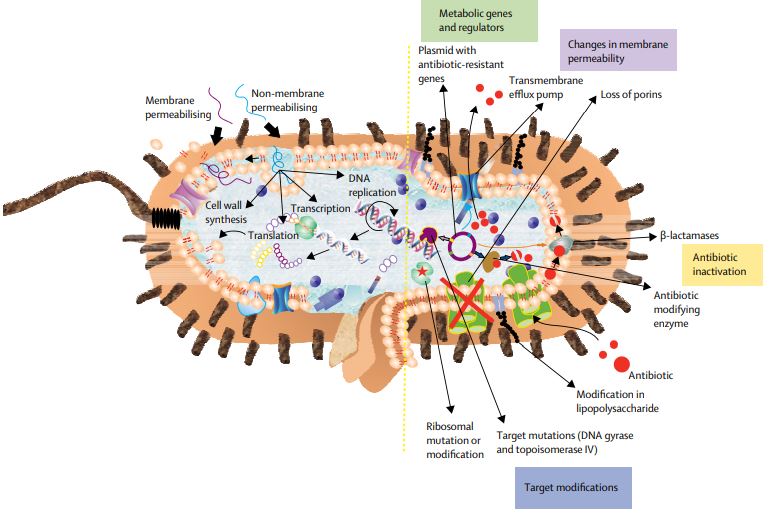
Antimicrobianos β-Lactâmicos
Desde a descoberta da penicilina, o grupo dos β-lactâmicos tem sido o mais utilizado no tratamento de infecções bacterianas, por apresentarem um amplo espectro de ação, fornecer atividade bactericida e uma grande margem de segurança. Eles são quimicamente caracterizados pela presença de um anel β-lactâmico que se liga a partir do compartilhamento de elétrons com proteínas de ligação de penicilina, o qual modifica sua estrutura impedindo a bactéria de realizar sua função. Como consequência deste impedimento, as bactérias não conseguem formar a parede celular, resultando assim na lise bacteriana [3].
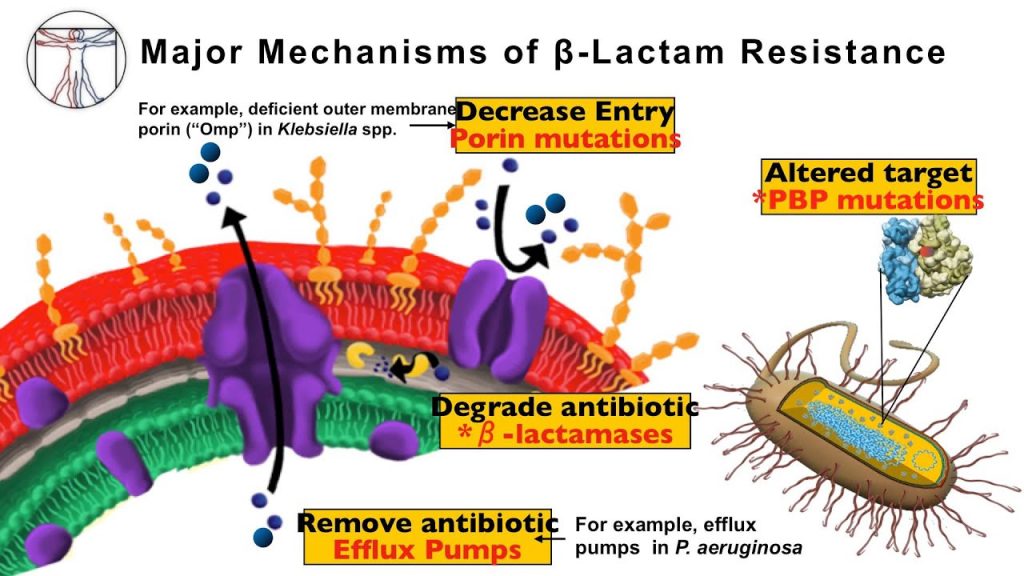
Apesar de compartilharem uma estrutura e um mecanismo de ação em comum, os β-lactâmicos são divididos em diferentes grupos de acordo com seus diferentes espectros de ação e estruturas químicas adicionais. Estes diferentes grupos são classificados como penicilinas, cefalosporinas, monobactâmicos, carbapenêmicos e inibidores de β-lactamases [4].
Penicilina
O grupo das penicilinas divide-se em: benzilpenicilinas (penicilinas naturais), penicilinas resistentes às penicilinases, aminopenicilinas e penicilinas de amplo espectro. O uso clínico do primeiro protótipo de antibiótico β-lactâmico teve início com a Penicilina G (benzilpenicilina) para o tratamento de infecções por estreptococos. São ativas frente a bactérias Gram-positivas a exemplo de Staphylococcus aureus, Streptococcus pneumoniae e Bacillus anthracis. No entanto, bactérias Gram-negativas são resistentes a ele [3]. As penicilinas podem ser classificadas em:Penicilina cristalina ou aquosa;
Penicilina G procaína;
Penicilina G benzatina;
Penicilina V.
A diferença entre elas está na forma como será administrada no paciente. Como podemos citar a Penicilina G procaína onde sua aplicação será administrada via intramuscular, já a Penicilina cristalina ou aquosa será por via endovenosa e com efeito mais rápido.
Penicilinas resistentes às penicilinases
São antibióticos bactericidas indicados principalmente para o tratamento de infecções por cepas de S. aureus produtoras de penicilinase. Eles atuam ligando-se às proteínas-ligadoras de penicilinas (PLPs), inibindo a síntese de componentes da parede celular bacteriana [5].
Aminopenicilinas
As aminopenicilinas são penicilinas semi-sintéticas, disponíveis desde 1960. Elas são adicionadas de um grupo amino na cadeia lateral e apresentam espectro de ação mais amplo, em relação às benzilpenicilinas. Os antibióticos mais conhecidos pertencentes a essa classe são amoxicilina e ampicilina,os quais foram sintetizados a partir de modificações na estrutura química das penicilinas naturais [3].
Penicilinas de Amplo Espectro
Apresentam um amplo espectro de atividade contra bactérias Gram-positivas e Gram-negativas, incluindo enterobactérias produtoras de β-lactamases de amplo espectro, o que os tornam uma alternativa para o tratamento de infecções graves [4].
Resistência antimicrobiana
Trata-se de um fenômeno natural onde há uma adaptação dos microrganismos através uma recombinação genética e/ou mutação. Ou seja, é uma habilidade que o microrganismo cria para sobreviver a concentrações de antimicrobianos que normalmente matariam células sensíveis. A exposição aos antimicrobianos utiliza uma pressão seletiva onde favorece o desenvolvimento de bactérias resistentes ou as tornam resistentes [6].
Mecanismo de resistência
Intrínseco = Quando ocorre a transferência de um gene resistente por meio da conjugação de uma bactéria para outra.
Extrínseco = Pode ocorrer a partir de uma mutação genética onde a bactéria pode adquirir resistência de forma espontânea ou induzida. Esse gene de resistência também pode ser adquirido a partir de uma recombinação genética por conjugação, transformação e transdução [7].
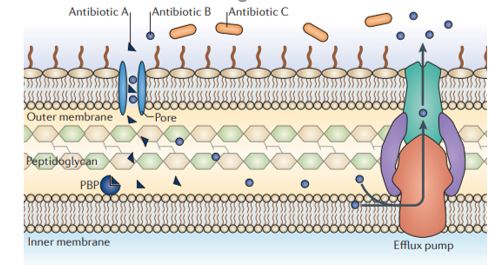
Figura 1-A figura mostra uma visão geral dos mecanismos de resistência intrínseca. O exemplo mostrado é de antibióticos β-lactâmicos direcionados a uma proteína de ligação à penicilina (PBP). O antibiótico A pode entrar na célula através de uma proteína porina que atravessa a membrana, atingir seu alvo e inibir a síntese de peptidoglicano. O antibiótico B também pode entrar na célula por meio de uma porina, mas, ao contrário do antibiótico A, é removido com eficiência por efluxo. O antibiótico C não pode atravessar a membrana externa e, portanto, não é capaz de acessar o PBP alvo [8].
Antibiograma
O antibiograma é um método eficiente utilizado para medição de sensibilidade de microrganismos a antibióticos. Esse tipo de técnica além de ajudar na escolha de terapia antimicrobiana, também é utilizado para mensurar mecanismos de resistência extrínseca [9]. Existem três tipos de antibiogramas: o para avaliação qualitativa, realizado a partir de testes de disco difusão em ágar; o para avaliação quantitativa, o qual pode ser realizado a partir de diluição em caldo, podendo ser macrodiluição ou microdiluição, ou diluição em ágar através do E-TEST; e, por fim, o automatizado.
Disco difusão
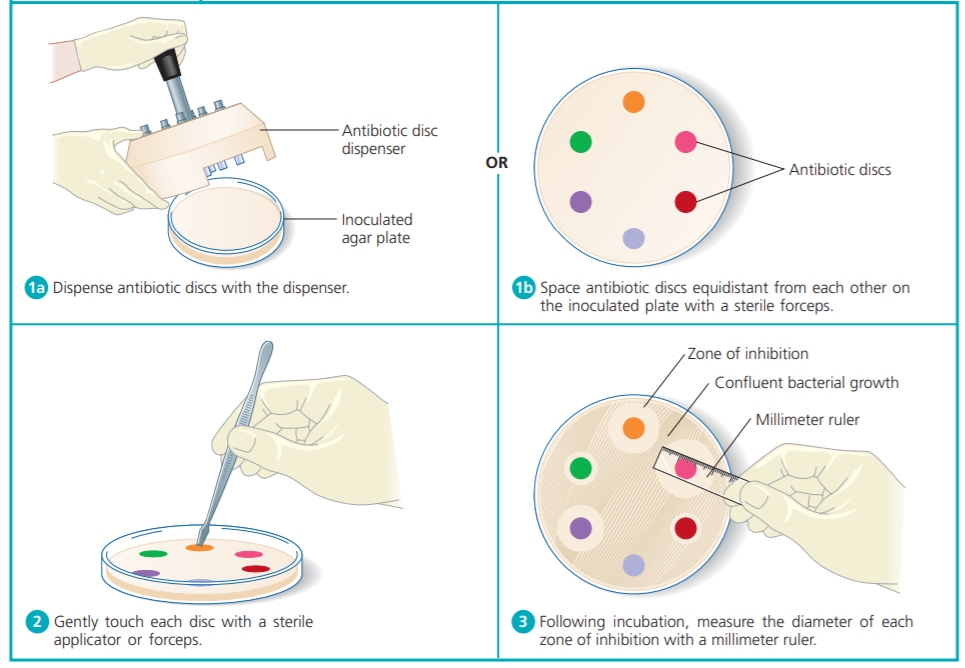
Figura 2-Experimento com disco de difusão.
Disco difusão é um método onde os testes são feitos in vitro, usando uma placa de petri com inoculação do microrganismo em ágar e posterior aplicação de disco de papel com o antibiótico. É uma técnica bastante utilizada devido à simplicidade, baixo custo e possibilidade de testes com grande número de microrganismos e antimicrobianos. A inibição pelo antibiótico será indicada através da formação de um halo [1].
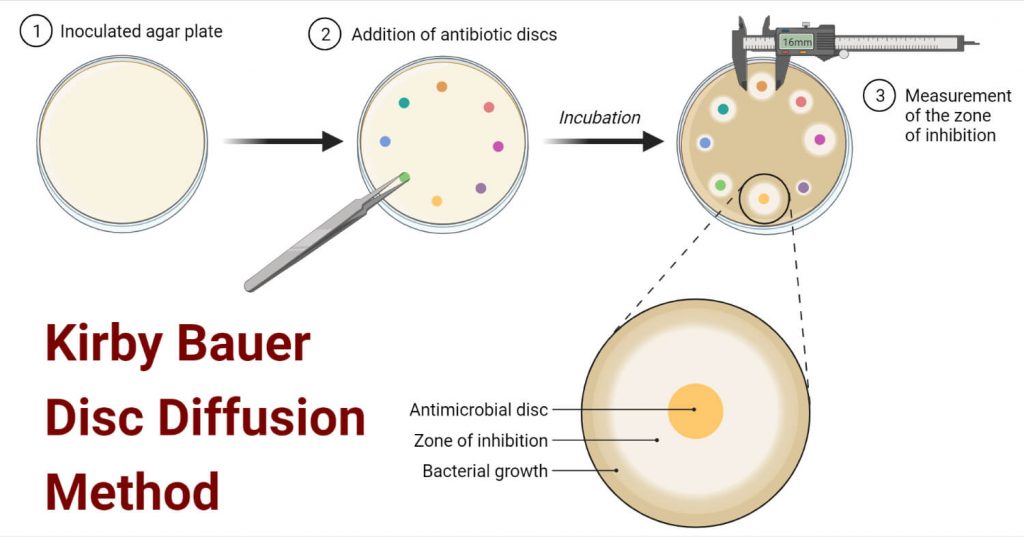
De acordo com a resistência ao antimicrobiano nesse teste, os microrganismos serão classificados em:
Sensível: É dada como sensível a um antimicrobiano quando houver inibição in vitro pela concentração da substância, assim tendo chances de ter efetividade terapêutica.
Intermediário: É considerado de resistência intermediária a um antimicrobiano quando ocorre uma inibição in vitro mas não existe uma certeza de que a droga utilizada teria resultados satisfatórios, assim, ficando incerto.
Resistente: É considerada resistente ao antibiótico quando não ocorre inibição in vitro e mostrado que a possibilidade de fracasso com a droga é alta, assim não sendo considerada para o uso no tratamento terapêutico.
Diluição em caldo
Microdiluição em caldo
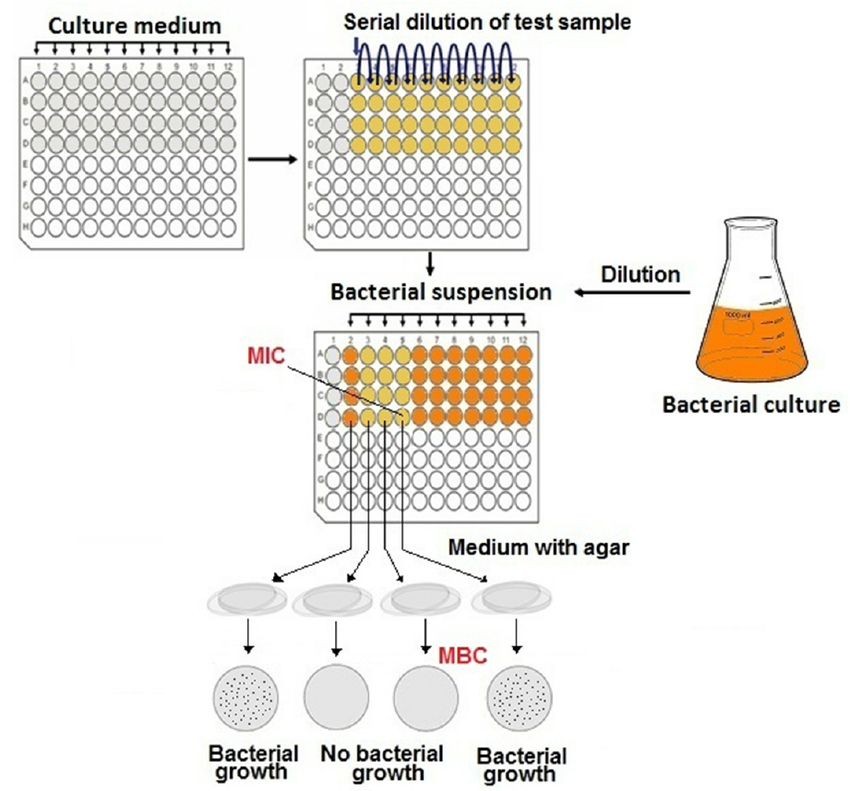
Trata-se de uma técnica quantitativa onde é realizada uma suspensão bacteriana com uma concentração pré-definida, normalmente ajustada a 0,5 na escala de McFarland. É diluída em caldo e testada contra diferentes concentrações de antimicrobiano. Todavia, é um método que requer muitas etapas e a sua preparação pode levar a erros significativos. Diante disso, é considerado um método não adaptável à rotina da maioria dos laboratórios de microbiologia [9].
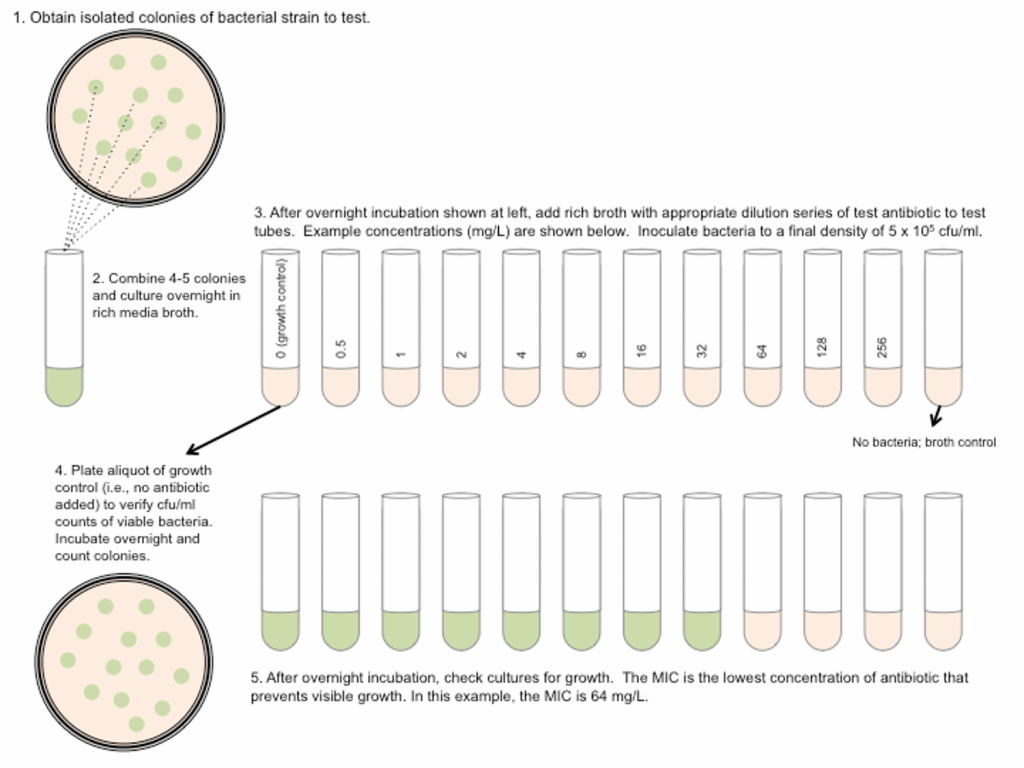
Macrodiluição em caldo
Conhecida como método de diluição em tubos, a macrodiluição em caldo é uma técnica parecida com a microdiluição em relação ao tempo de preparo, ao material usado e às características dos resultados. Essa técnica se diferencia por ser efetuada em tubos de ensaio, utilizando maior quantidade de caldo. Todos os tubos conterão concentrações diferentes dos antibióticos que serão usados e avaliados posteriormente [10].
Diluição em ágar
A diferença dessa técnica com a de diluições em caldo é basicamente a adição do antimicrobiano ao meio de cultura antes mesmo que ele solidifique na placa de petri. Nessa técnica, são preparadas várias placas com diferentes concentrações do antimicrobiano e após efetuar semeio da bactéria a ser testado, o material é incubado em estufa. O tempo e a temperatura de incubação variam de acordo com a bactéria e os antimicrobianos que serão testados.
Após o tempo estabelecido, é feita uma avaliação visual das placas, sendo o antimicrobiano efetivo quando não há crescimento bacteriano na placa. Uma vantagem dessa técnica é que se pode efetuar o teste de vários isolados por placa. Como desvantagem, tem-se o tempo de realização, quando não é realizado de forma automatizada.
REFERÊNCIAS
- CORRÊA, A. J. C. (2018). Contribution of popular knowledge to the discovery of new antimicrobials. 2018.
- Magana, M., Pushpanathan, M., Santos, A. L., Leanse, L., Fernandez, M., Ioannidis, A., … Tegos, G. P. (2020). The value of antimicrobial peptides in the age of resistance. The Lancet Infectious Diseases. doi:10.1016/s1473-3099(20)30327-3
- LIMA, L. M. et al. (2020) β-lactam antibiotics: An overview from a medicinal chemistry perspective. European Journal of Medicinal Chemistry, p. 112829, 2020.
- SILVA, Q. M. (2017). Resistência bacteriana a antimicrobianos em uma comunidade remota da Floresta Amazônica. Tese de Doutorado. Universidade de São Paulo.
- WOLLHEIM, C. (2014). Epidemiologia molecular de Escherichia coli e Klebsiella spp produtoras de beta-lactamase de espectro ampliado. Tese de doutorado. Universidade de Caxias do Sul.
- DROPA, M. (2012). Disseminação da resistência a antimicrobianos em cepas clínicas e ambientais de Enterobacteriaceae: identificação e mapeamento do ambiente genético de genes codificadores de ESBL. 2012. Tese de Doutorado. Universidade de São Paulo.
- COX, G..; WRIGHT, D. G. (2013). Intrinsic antibiotic resistance: mechanisms, origins, challenges and solutions. International Journal of Medical Microbiology, v. 303, n. 6-7, p. 287-292.
- BLAIR, J., WEBBER, M., BAYLAY, A. et al. (2015). Molecular mechanisms of antibiotic resistance. Nat Rev Microbiol,13, 42–51.
- HUGHES, M. A. et al. (2020). Antibiograms Cannot be used interchangeably between acute care medical centers and affiliated nursing homes. Journal of the American Medical Directors Association, v. 21, n. 1, p. 72-77.
- GOULART, T. M.(2017). Comparação entre Etest® e microdiluição em caldo para avaliação da susceptibilidade à polimixina B em Klebsiella pneumoniae produtoras de KPC. Trabalho de conclusão de curso. Universidade Federal do Rio Grande do Sul.