Olá pessoal, tudo bem com vocês? Hoje no Blog vamos bater um papo sobre a Imunologia viral, principalmente em relação a COVID – 19.
Você já ouviu falar sobre esse assunto?
Lembra que os últimos artigos nos abordamos sobre imunologia e hoje falaremos mais um pouco sobre Imunologia viral.
Imunologia viral
Respostas imunes tanto inatas e adaptativas contra os vírus, assim como viemos aprendendo tem o intuito de bloquear a infecção e eliminar as células infectadas.
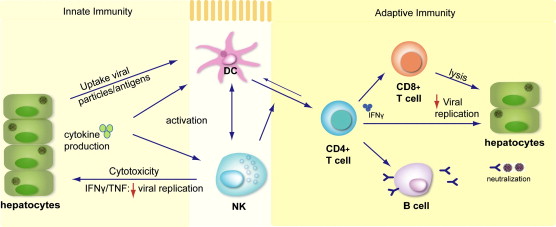
A maioria da resposta para prevenir a infecção é mediada por interferons do tipo I como parte da imunidade inata e os anticorpos neutralizantes na imunidade adaptativa.
No entanto, quando a infecção é estabelecida, as células infectadas por esses vírus serão eliminadas pelas células NK na resposta inata e pelo Linfócito CD8+ citotóxico (CTL) na resposta adaptativa.
Agora vamos entender de maneira geral como cada uma dessas respostas funcionam??
Imunidade Inata contra Vírus
Os principais mecanismos de imunidade inata contra os vírus são mediados pela produção de interferons do tipo I por um grupo de células dendríticas e a destruição das células infectadas ocorrerá pelas células NK.
Essas células dendríticas para produzir esse interferon precisa ser previamente ativada, essa ativação se dá pelo reconhecimento de RNA e DNA viral pelos TLRs endossomais e ativação de receptores citoplasmáticos tipo RIG e da via de STING (sigla do inglês Stimulator of interferon genes) pelo RNA e DNA virais, respectivamente, o que culminarão na transcrição do gene de interferon tipo I.
Esses interferons tipo I têm a capacidade de inibir a replicação viral em ambas as células infectadas e não infectadas. Assim como levar a ativação de células que auxiliem na contenção da infecção.
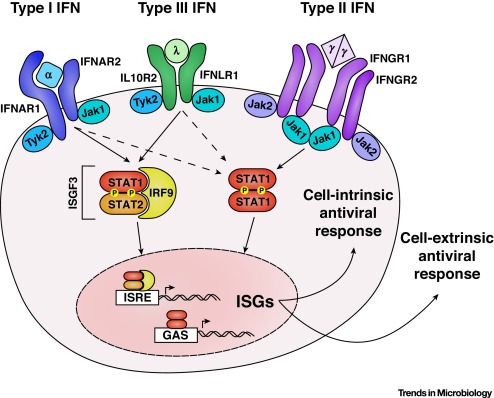
A ativação das células NK, principais células com capacidade citotóxica na imunidade inata, se dá por um complexo equilíbrio entre sinais inibidores e ativadores que atuam em seus receptores, assim como também se dá pela presença ou ausência das moléculas do complexo maior de histocompatibilidade classe I (MHC classe I). Sabe-se que muitos vírus conseguem desligar a expressão do MHC de classe I como um mecanismo de evasão dos linfócitos CD8+ citotóxicos, isso acaba permitindo que as células NK destruam essas células infectadas devido à ausência do MHC classe I.
Após a ligação às células alvo, as células NK irão produzir perforinas que originam vários poros na membrana celular resultando na sua lise celular. Essa lise celular ainda pode ser potencializada pela atuação de citocinas como: IL-2, IFN-γ, TNF-α, TNF-β capazes de gerar um efeito sinérgico nessa ação citotóxica.

Durante essa ação a resposta imune adaptativa está sendo ativada…
Imunidade Adaptativa contra vírus
A imunidade adaptativa contra os vírus é mediada através de anticorpos e da atuação dos linfócitos T CD8+ citotóxicos.

Quando mediada pelos anticorpos estes possuem o papel de bloquear/ neutralizar a ligação do vírus com os receptores que permitirão a entrada do mesmo na célula hospedeira. Para que isso aconteça esses anticorpos precisam ser produzidos através da resposta humoral dependentes de células T.
Vale ressaltar que esses anticorpos só são eficazes durante a fase extracelular dos vírus, ou seja, no inicio do curso da infecção antes que infectem as células hospedeiras ou quando são liberados para infectar demais células.
O principal papel desses anticorpos como dito é a neutralização, no entanto a opsonização também podem auxiliar levando a fagocitose dessas partículas e consequente eliminação.
Já os CTLs eliminam a infecção matando diretamente as células infectadas. A principal função fisiológica dos CTLs é a vigilância contra infecção viral. A maioria dos CTLs específicos para vírus são células T CD8 + que reconhecem peptídeos virais, citosólicos, geralmente sintetizados endogenamente e que são apresentados por moléculas de classe I do MHC.
Se a célula infectada é uma célula de tecido e não uma célula apresentadora de antígenos profissional (APC), tais como células dendríticas, a célula infectada pode ser fagocitada pelas células dendríticas, que processarão os antígenos virais e assim apresentarão para as células T imaturas.
A diferenciação completa de CTLs CD8 + muitas vezes dependem de citocinas produzidas pelas células T CD4 + auxiliares ou os coestimuladores expressos nas células infectadas.
Os efeitos antivirais de CTLs são principalmente devidos à morte de células infectadas, com a atuação de perforinas e granzinas que promovem a autólise da célula infectada. No entanto, outros mecanismos incluem a ativação de nucleases dentro de células infectadas que degradam genomas virais e a secreção de citocinas, tais como IFN-γ, que ativa fagócitos pode apresentar alguma atividade antiviral.
Nos últimos anos há relatos que as células TCD4+ auxiliares também são capazes de produzir essas perforinas e granzinas e atuarem de maneira similar as CTLs.
Certo, após compreendermos o mecanismo de ação da imunidade viral, vamos compreender como se dá frente ao SARS-CoV-2?
Primeiramente, vamos iniciar falando um pouquinho sobre o SARS-CoV-2.

O SARS-CoV-2 é o agente etiológico da síndrome respiratória aguda grave a COVID-19, grave doença classificada como enfermidade epidêmica amplamente disseminada, que consequentemente resultou em morbidade e mortalidade generalizadas em todo o mundo, resultando assim na pandemia atual.
Apresenta diversas formas de transmissão, destacando-se as gotículas salivares produzidas em: tosses, conversas, espirros, como também o contato com outros indivíduos.
Por isso, o indivíduo infectado consegue transmitir a COVID-19, nos primeiros três dias após os sintomas iniciais, mas, a propagação pode ocorrer antes do aparecimento de quaisquer sintomas e também em estágios posteriores da doença. Entre a exposição ao vírus e o início dos sintomas existe um prazo de cinco dias, tempo este denominado de incubação, porém, o intervalo pode variar de 2 a 14 dias.
O SARS-COV-2 é considerado um vírus envelopado de RNA fita simples positiva, que varia de 50 a 200nm, sendo o mais novo coronavírus humano identificado.
Como outros coronavírus, o mesmo apresenta quatro proteínas estruturais, sendo elas: a proteína spike (S), a proteína do envelope (E), a proteína do nucleocapsídeo (N) e também a proteína de membrana (M). Dentre essas proteínas, a Spike é a que determina a interação com a célula hospedeira promovendo assim adesão e fusão do vírus com a membrana plasmática.
Dentre os diversos sintomas destacam-se: tosse seca, falta de ar e febre. Com isso alguns pacientes, requerem hospitalização caso desenvolvam quadros mais severos da doença como: insuficiência respiratória hipoxêmica, choque séptico e pneumonia.
Problemas neurológicos, incluindo mau funcionamento do tronco cerebral, ocorrem em alguns pacientes e podem estar associados a insuficiência respiratória, mesmo na ausência de dano pulmonar difuso.
Problemas nefrológicos e gastrointestinais também foram relatados, e a co-ocorrência dessas patologias pode levar à falência de múltiplos órgãos. No entanto, o dano pulmonar isolado parece ser a principal causa de fatalidade do COVID-19.
O dano ao órgão ou tecido ocasionado pela COVID-19 está associado a uma inflamação sistêmica e à chamada “síndrome de liberação de citocinas” (sigla do inglês SRC – cytokine release syndrome).
Embora esse vírus tenha a capacidade de causar danos diretos aos tecidos epiteliais por meio de lesão e necrose dessas células, evidências indicam que esses danos estão associados a ativação do sistema imune.
Alguns estudos em pacientes com COVID-19 mostraram que o vírus desencadeia a produção elevada de vários mediadores inflamatórios, incluindo citocinas inflamatórias que são produzidas principalmente por monócitos e macrófagos no caso do pulmão, os macrófagos alveolares são os responsáveis pelo aumento dessas citocinas locais devido ao grande número de partículas virais que ali se encontram.
Resposta inata contra COVID-19
Assim que os vírus entram no tecido do hospedeiro o processo inflamatório dará início a imunidade inata. Com isso, os PAMPs virais irão ativar os PRRs para que assim as células que compõe a imunidade inata sejam ativadas.
Os PAMPs associados ao SARS-CoV incluem ssRNA genômico viral e substâncias intermediárias produzidas durante a replicação viral, ou seja, dsRNA, bem como proteínas virais.
As moléculas de ssRNA e dsRNA de coronavírus podem ser detectadas por vários PRRs endossômicos ou citosólicos.
Destacam-se os TLR3 endossômico e TLR7 endossômico. Da mesma forma, os sensores de RNA citoplasmático, RIG-I e o gene 5 associado à diferenciação do melanoma, respondem aos RNAs do coronavírus.

Alguns estudos sobre o SARS-CoV e o MERS-CoV demonstraram que a sinalização mediada por RIG-I é muito importante na indução de respostas antivirais do interferon contra esses vírus. O STING mesmo normalmente estando associado a presença de DNA citosólico e, embora os coronavírus não tenham DNA, a sinalização mediada por STING foi relatada na literatura após infecções por coronavírus.
As proteínas virais também vão servir como PAMPs. A proteína spike SARS-CoV é conhecida por interagir com o TLR-2. A proteína M SARS-CoV também atua como um PAMP citosólico e induz respostas de interferon relacionadas a TLR.
Essas interações PAMP-PRR irão resultar na ativação de fatores de transcrição “promotores de inflamação” (TF), incluindo o fator nuclear kappa B (NF-κB) e o fator regulador de IFN 3 (IRF3). Esses fatores de transcrição irão promover a produção dos interferons do tipo I, importantes para a imunidade viral, assim como outras citocinas pró-inflamatórias também serão produzidas.
Quando se compara a infecção do SARS-CoV-2 com outros vírus respiratórios, percebe-se uma ativação da imunidade viral mais leve, marcada com baixas produções de interferons gama do tipo I, no entanto, o aumento de quimiocinas é maior, o que pode explicar o estado de uma doença pró-inflamatória.
No início da infecção a replicação viral acontece rapidamente sem muita produção de IFNs, a isso acredita-se que seja atribuído a proteínas não estruturais conservadas presentes no vírus.
O aumento das quimiocinas como dito acima leva a um influxo de neutrófilos e monócitos no local da inflamação sendo mediares pró-inflamatórios, contribuindo para o aumento dos níveis de citocinas pró-inflamatória, esse efeito tem sido denominado como tempestade de citocinas.

Imunidade Adaptativa contra COVID-19
Assim como descrito acima a resposta imune adaptativa contra vírus pode ser dividida em humoral e celular. Os anticorpos neutralizantes são os principais protetores no ambiente extracelular, enquanto as células T citotóxicas CD8 + têm um papel proeminente contra os vírus intracelulares. Ambos os elementos são controlados e regulados por células T CD4 + específicas do antígeno.
Resposta imune humoral
Estudos recentes sobre respostas de anticorpos em pacientes com COVID-19 demonstraram que a maioria dos pacientes desenvolve anticorpos IgM e / ou IgG específicos para vírus logo após a infecção. Estudos mostram que em alguns pacientes os anticorpos eram detectáveis logo 4 dias após o início dos sintomas. Se esses anticorpos ainda são responsáveis pela proteção ainda não se sabem.
No entanto, alguns estudos verificaram que a transferência de plasma contendo esses anticorpos neutralizantes melhoraram a recuperação de pacientes com COVID-19.
Além da atividade neutralizante, a ativação do complemento por anticorpos específicos para vírus é outra funcionalidade que deve ser considerada no contexto de uma resposta imune humoral. No entanto, há evidências indicando que a ativação do complemento contribui para a patogênese do coronavírus. Um estudo de Magro et al. demonstrou que a ativação do complemento aumenta a lesão microvascular e a trombose em casos de COVID-19.
Outro ponto importante é um fenômeno denominado “realce dependente de anticorpos” o qual se trata de um processo pelo qual a ligação de um anticorpo não neutralizante facilita a entrada do vírus nas células e é provável que esse fator contribua para o aumento da replicação viral e virulência.
Este fenômeno foi relatado para outros vírus, incluindo coronavírus, e no caso do SARS-CoV-2 já foi relatado que anticorpos contra a proteína Spike contribuem para esse efeito.
Resposta imune celular
As células citotóxicas CD8 + específicas para vírus representam a parte efetora da imunidade mediada por células contra vírus. No entanto, a sua atividade, bem como a atividade das células B, é estreitamente regulada pelas células T auxiliares CD4 +, que são posteriormente divididas em fenótipos funcionais Th1, Th2, Th9, Th17 e Treg.
As informações sobre as respostas imunes celulares protetoras em COVID-19 são limitadas. Porém, de acordo com a análise de células sanguíneas periféricas em pacientes com COVID-19 o número de células T CD4 + e CD8 +, assim como células B e células NK foi reduzido, especialmente em casos mais graves.
Contudo, esses números reduzidos não significam necessariamente redução da atividade celular, pois podem indicar que essas células podem estar em um estado hiperativado.
Mas o que isso quer dizer?
Um estudo para verificar uma imunofenotipagem analisou alguns receptores e a presença deles era numerosa o que podia indicar que a expressão desses receptores pode ser consequência da exaustão das células T ou devido ao alto nível de ativação das células T.
Em relação as células T CD4 + específicas para a proteína Spike nota-se uma reposta grave quando o perfil da resposta é Th17, aguda quando apresenta um perfil de citocinas de células Th1 e leve quando apresenta um perfil Th2. Ainda não está claro a eficácia desses subconjuntos de células T CD4 + e CD8 + na proteção contra a infecção por COVID-19.
Conclusão
No artigo de hoje trouxemos a imunidade viral e os relatos na literatura sobre como tem sido descrito a imunidade viral contra a COVID-19. Como foi visto, o nosso sistema imunológico tem um papel muito importante no combate ao SARS-CoV-2, assim como na gravidade da doença, devido a tempestade de citocinas que é visto nos casos mais graves. Muito ainda tem a se descobrir.
Espero que vocês tenham gostado!!
Compartilhem com os colegas e deixem seu comentário.
Referências
- C. Magro, J.J. Mulvey, D. Berlin, G. Nuovo, S. Salvatore, J. Harp, A. Baxter-Stoltzfus, J. Laurence. Complement associated microvascular injury and thrombosis in the pathogenesis of severe COVID-19 infection: a report of five cases. Trans. Res.: J. Lab. Clin. Med. (2020)
- D.F. Robbiani, C. Gaebler, F. Muecksch, J.C. Lorenzi, Z. Wang, A. Cho, M. Agudelo, C.O. Barnes, A. Gazumyan, S. Finkin, Convergent antibody responses to SARS-CoV-2 infection in convalescent individuals, bioRxiv (2020).
- Dai, L., George F. G. “Viral targets for vaccines against COVID-19.” Nature Reviews Immunology. 2020.
- E. de Wit, N. van Doremalen, D. Falzarano, V.J. Munster. SARS and MERS: recent insights into emerging coronaviruses. Nat. Rev. Microbiol., 14 (8) (2016), p. 523
- E. Kindler, V. Thiel, F. Weber. Interaction of SARS and MERS Coronaviruses with the Antiviral Interferon Response. Adv. Virus Res., 96 (2016), pp. 219-243
- F. Wang, J. Nie, H. Wang, Q. Zhao, Y. Xiong, L. Deng, S. Song, Z. Ma, P. Mo, Y. Zhang. Characteristics of peripheral lymphocyte subset alteration in COVID-19 pneumonia. J. Infect. Dis. (2020)
- K.L. Siu, M.L. Yeung, K.H. Kok, K.S. Yuen, C. Kew, P.Y. Lui, C.P. Chan, H. Tse, P.C. Woo, K.Y. Yuen, D.Y. Jin. Middle east respiratory syndrome coronavirus 4a protein is a double-stranded RNA-binding protein that suppresses PACT-induced activation of RIG-I and MDA5 in the innate antiviral response. J. Virol., 88 (9) (2014), pp. 4866-4876
- L. Sun, Y. Xing, X. Chen, Y. Zheng, Y. Yang, D.B. Nichols, M.A. Clementz, B.S. Banach, K. Li, S.C. Baker, Z. Chen. Coronavirus papain-like proteases negatively regulate antiviral innate immune response through disruption of STING-mediated signaling. PLoS ONE, 7 (2) (2012).
- M.S. Yip, N.H. Leung, C.Y. Cheung, P.H. Li, H.H. Lee, M. Daeron, J.S. Peiris, R. Bruzzone, M. Jaume. Antibody-dependent infection of human macrophages by severe acute respiratory syndrome coronavirus. Virol. J., 11 (2014), p. 82
- Male, D. et al. Imunologia. Grupo GEN, 2014.
- Oliveira, E. H. A. Coronavírus: prospecção científica e tecnológica dos fármacos em estudo para tratamento da COVID – 19. Cadernos de Prospecção – Salvador, v. 13, n. 2, p. 412-423, 2020.
- S.F. Dosch, S.D. Mahajan, A.R. Collins. SARS coronavirus spike protein-induced innate immune response occurs via activation of the NF-kappaB pathway in human monocyte macrophages in vitro. Virus Res., 142 (1–2) (2009), pp. 19-27.
- S.F. Wang, S.P. Tseng, C.H. Yen, J.Y. Yang, C.H. Tsao, C.W. Shen, K.H. Chen, F.T. Liu, W.T. Liu, Y.M. Chen, J.C. Huang. Antibody-dependent SARS coronavirus infection is mediated by antibodies against spike proteins. Biochem. Biophys. Res. Commun., 451 (2) (2014), pp. 208-214
- S.W. Li, C.Y. Wang, Y.J. Jou, S.H. Huang, L.H. Hsiao, L. Wan, Y.J. Lin, S.H. Kung, C.W. Lin. SARS Coronavirus Papain-Like Protease Inhibits the TLR7 Signaling Pathway through Removing Lys63-Linked Polyubiquitination of TRAF3 and TRAF6. Int. J. Mol. Sci., 17 (5) (2016)
- SETTE, A.; CROTTY, S. Adaptive immunity to SARS-CoV-2 and COVID-19. Cell, 2021.
- Souto, X. M. Covid-19: aspectos gerais e implicações globais. Revista de Educação, Ciência e Tecnologia de Almenara, v. 2, n. 1, 2020.
- Totura, A. Whitmore, S. Agnihothram, A. Schafer, M.G. Katze, M.T. Heise, R.S. Baric. Toll-Like Receptor 3 Signaling via TRIF Contributes to a Protective Innate Immune Response to Severe Acute Respiratory Syndrome Coronavirus Infection. mBio, 6 (3) (2015), pp. e00638-e00715
- W.J. Liu, M. Zhao, K. Liu, K. Xu, G. Wong, W. Tan, G.F. Gao.T-cell immunity of SARS-CoV: Implications for vaccine development against MERS-CoV. Antiviral Res., 137 (2017), pp. 82-92
- 19. Wajnberg, A., et al. “Robust neutralizing antibodies to SARS-CoV-2 infection persist for months.” Science. p.370.6521, 2020.



Sensacional, super interessantes as informações.